化学常用计量(释疑解惑)
问题1:物质的量与质量、微粒数、气体的体积以及物质的量浓度之间是什么关系?用公式表示。这些公式中哪些需要条件?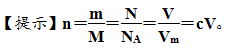 气体的体积与物质的量之间的关系,是通过Vm建立的,而Vm与外界的条件(温度、压强)有很大关系。
气体的体积与物质的量之间的关系,是通过Vm建立的,而Vm与外界的条件(温度、压强)有很大关系。问题2:在标准状况下,1 mol 任何物质所具有的体积约为22.4 L吗?
【提示】错误。“物质”应改成“气体”。试题中常考的液体有H2O、CH3CH2OH、CCl4、苯、戊烷(碳原子数大于4的烃)、HF等,常考的固体有SO3。
特别提醒:HCHO、CH3Cl属于气体。
问题3:①浓度为1 mol·L-1的Na2CO3溶液中含有NA个CO3吗?②25 ℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA,正确吗?
【提示】①错误,因为题中没有指明溶液的体积,故无法计算出溶液中离子的数目,且CO3会发生水解,故其数目要减少。②错误,pH=13的1.0 L Ba(OH)2溶液,电离出的OH-总浓度为0.1 mol·L-1,无需再扩大2倍。
问题4:①标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA吗?②0.1 mol N2与足量H2反应,转移的电子数为 0.6NA吗?
【提示】①错误。因为Cl2溶于水为可逆反应,故转移电子数应小于0.1NA。②不正确。因为N2与H2反应为可逆反应,故不可能完全反应,转移的电子数小于0.6NA。
问题5:①0.1 mol羟基(···H )中含有的电子数为0.7NA吗?②0.1 mol氢氧根(OH-)中含有的电子数为0.9NA吗?
【提示】1个羟基中含有9个电子,羟基为中性,故0.1 mol羟基(···H )中含有的电子数为0.9NA,①错误。1个氢氧根(OH-)中含有10个电子,故0.1 mol OH-中含有的电子数为NA,②错误。



发表评论 取消回复