重要的工业反应与常见工艺流程(典型例题)
规律总结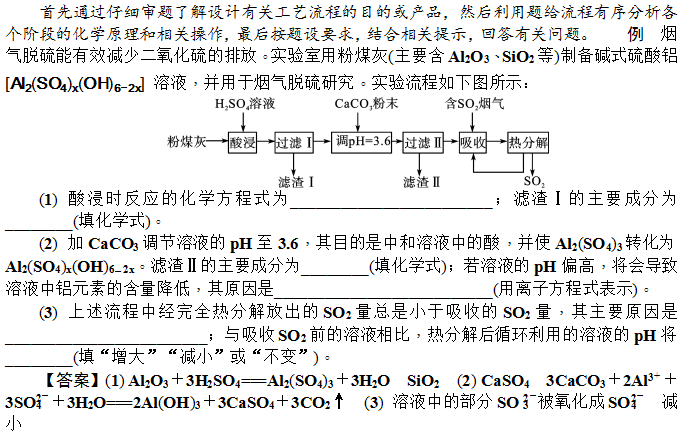 【解析】(1) 粉煤灰中的Al2O3能与H2SO4反应生成Al2(SO4)3,而SiO2不与H2SO4反应,因而滤渣Ⅰ为SiO2。(2)滤液Ⅰ为Al2(SO4)3溶液,与CaCO3反应生成微溶物CaSO4,因而滤渣Ⅱ为CaSO4;向滤液Ⅰ中加入CaCO3粉末的目的是中和溶液中的酸,若溶液的pH偏高,碱性增强,会促进Al3+水解,铝元素容易转化为Al(OH)3沉淀而导致溶液中铝元素含量降低。(3) +4价S具有较强还原性,溶液中的SO3容易被氧化为SO4。SO2在水中溶解度较大且SO2溶于水生成H2SO3,且加热时部分H2SO3会被氧化为酸性更强的H2SO4,故热分解后循环利用的溶液的pH将减小。
【解析】(1) 粉煤灰中的Al2O3能与H2SO4反应生成Al2(SO4)3,而SiO2不与H2SO4反应,因而滤渣Ⅰ为SiO2。(2)滤液Ⅰ为Al2(SO4)3溶液,与CaCO3反应生成微溶物CaSO4,因而滤渣Ⅱ为CaSO4;向滤液Ⅰ中加入CaCO3粉末的目的是中和溶液中的酸,若溶液的pH偏高,碱性增强,会促进Al3+水解,铝元素容易转化为Al(OH)3沉淀而导致溶液中铝元素含量降低。(3) +4价S具有较强还原性,溶液中的SO3容易被氧化为SO4。SO2在水中溶解度较大且SO2溶于水生成H2SO3,且加热时部分H2SO3会被氧化为酸性更强的H2SO4,故热分解后循环利用的溶液的pH将减小。


发表评论 取消回复