电解原理及其应用(典型例题)
规律总结
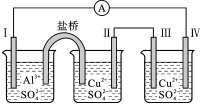
原电池与电解池的明显区别在于原电池作电源,电解池需有外加电源。在原电池中,失电子发生氧化反应的为负极,得电子发生还原反应的为正极。在电解池中,接电源正极的发生氧化反应作阳极,接电源负极的发生还原反应作阴极。在原电池中,活泼金属通常作负极,首先被腐蚀,不活泼金属作正极,被保护不受腐蚀,这种金属保护法也称作牺牲阳极的阴极保护法。在电解池中,阴极金属被保护,这种金属保护法也称作外加电源的阴极保护法。 例 某同学组装了如图所示的电化学装置,电极Ⅰ为Al,其他电极均为Cu,则( )



发表评论 取消回复